Explorando el universo oculto de los ARN: el fascinante mundo de los micropéptidos
Introducción
Inherente a la complejidad del cuerpo humano, existe una gran variedad de moléculas que interaccionan continuamente dentro y fuera de las células. Múltiples disciplinas han tratado de comprender este mundo complejo, mediante el estudio de diversas biomoléculas como las proteínas, carbohidratos, lípidos y los ácidos nucleicos, incluyendo al ácido desoxirribonucleico (ADN) y al ácido ribonucleico (ARN). Sin embargo, aun con todos los avances de la ciencia, persisten piezas desconocidas en este rompecabezas molecular; aquí abordaré una de estas piezas que se relaciona específicamente con el ARN.
Para iniciar, debe recordarse que se han identificado varios tipos de ARN como el ARN mensajero, el ribosomal y el de transferencia. De manera muy sencilla, los ARN mensajeros, que son una copia de regiones específicas de ADN, contienen las instrucciones necesarias para generar proteínas, también denominadas polipéptidos. En este proceso de construcción de proteínas participan el ARN ribosomal y de transferencia. El primero forma parte de las fábricas –mejor conocidas como ribosomas– que producen proteínas, involucrándose directamente en la unión de dos aminoácidos mediante el enlace peptídico. Por su parte, los ARN de transferencia se encargan de transportar los aminoácidos que serán las piezas para armar las proteínas.
En la actualidad tenemos conocimiento de la existencia de otras especies de ARN como son los ARN largos no codificantes, que como su nombre lo indica, no contienen información para producir proteínas, pero que realizan múltiples funciones relevantes dentro de la célula. Estos ARN se caracterizan por tener una longitud mayor a 200 pares de bases. A la fecha se ha logrado identificar alrededor de 56,000 ARN largos no codificantes, aunque la cifra podría ser mayor. Su importancia se refleja en las funciones en las que intervienen, destacando su papel como reguladores de la transcripción, de la actividad de proteínas y de los cambios epigenéticos, es decir, aquellas modificaciones que no alteran la secuencia del ADN, pero sí la manera en que este se expresa. Dentro de esta diversidad de funciones, resalta que se ha encontrado la excepción a la regla, es decir, que en realidad algunos de estos ARN largos “no codificantes”, sí contienen información para generar micropéptidos.
Los micropéptidos
Los micropéptidos son pequeños péptidos de hasta 100 aminoácidos, un valor arbitrario. Se diferencian de los péptidos ampliamente estudiados como la insulina y glucagón, porque las instrucciones para su producción están en varios de los ARNs mal denominados no codificantes. Es decir, a diferencia de los péptidos comunes, no provienen de una proteína producida por más de 100 aminoácidos que fue procesada –eliminación de aminoácidos– para generarlos (Figura 1).
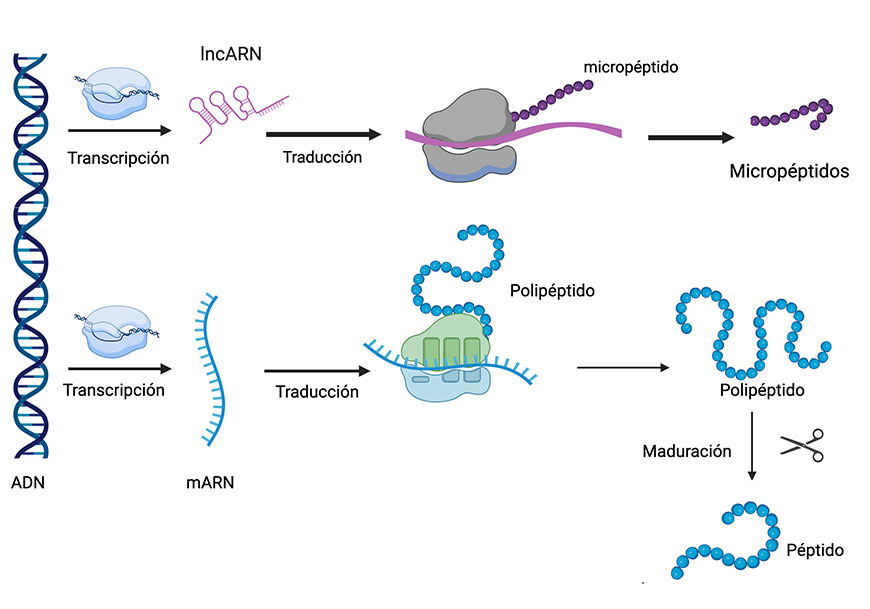
Figura 1. Origen de micropéptidos a partir de lncARN. El lncARN contiene un marco de lectura abierto corto (MLAc) que es leído por el ribosoma, dando lugar a un micropéptido. Éstos se diferencian de los péptidos convencionales porque solo provienen de la traducción del lncARN, en lugar de ser el resultado de la maduración (corte) de un polipéptido mayor de 100 aminoácidos.
Un ejemplo sencillo es el caso de la insulina, que inicialmente se produce como una proteína de 110 aminoácidos; posteriormente, para que sea funcional y logre hacer su trabajo de regular la glucosa en la sangre, debe sufrir un procesamiento post-traduccional a su paso por el retículo endoplásmico rugoso – organelo con numerosos ribosomas adheridos–, y posteriormente por el aparato de Golgi. Así, tras la eliminación de 59 aminoácidos, la insulina queda conformada por 51 aminoácidos organizados en las dos cadenas unidas entre sí por puentes disulfuro. En contraste, los micropéptidos se producen sin necesidad de procesamiento posterior, a la medida perfecta requerida para su función.
Para una mejor comprensión, en este momento es necesario hablar sobre los marcos de lectura abiertos. La sección de un ARN mensajero que contiene la información para el orden de los aminoácidos de una proteína, se conoce como marco de lectura abierto (MLA). El Consorcio Internacional de Científicos que llevó a cabo el Proyecto del Genoma Humano definió que los MLAs debían tener un tamaño mayor a 300 pares de bases –>100 codones– para eliminar falsos positivos. Con este supuesto, lograron identificar que cerca del 2-3% del genoma son genes que codifican a proteínas.
No obstante, estudios exhaustivos para comprender la complejidad del genoma humano han encontrado evidencia experimental sobre MLA menores a 300 pares de bases, denominados marcos de lectura abiertos cortos (MLAc). Así, estos MLAc son los que dan origen a los micropéptidos. En la actualidad se han identificado MLAc no solo en los ARN largos no codificantes, sino también en otros ARN, como los ARN circulares y ARN mitocondrial, entre otros.
El descubrimiento de los micropéptidos
En 2004, después de más de una década de trabajo del Consorcio Internacional de Científicos, se dio a conocer la secuencia completa del material genético, el ADN que nos identifica como especie. Las primeras conclusiones fueron que solo entre el 2-3% de la información contenida en el genoma se utilizaba para generar proteínas y que el restante parecía ADN “basura”. Empero, muchos investigadores con base en el principio de que la célula no desperdicia energía, se negaron a aceptar esa idea simplista y comenzaron a estudiar la función del ADN “basura”.
En la actualidad, tras múltiples investigaciones, se ha determinado que la gran mayoría del ADN “basura” tiene una función, por ejemplo, contiene la información para producir ARN largos no codificantes. Estos ARN fueron denominados así por no tener en apariencia, información necesaria para sintetizar proteínas. Diversos grupos de científicos se han dado a la tarea de reconocer su papel dentro de las células u organismos. Para ello se han utilizado diferentes estrategias metodológicas, como la biología computacional, análisis de transcriptomas –esto es, la colección completa de ARN que producen las células– y de proteomas que corresponden al conjunto total de proteínas presentes en ellas.
Entre los hechos más relevantes acerca de los ARN no codificantes y que han resultado controversiales entre la comunidad científica, es que algunos de ellos contienen información para generar pequeños péptidos menores a 100 aminoácidos. La convención actual para nombrar a estos pequeños péptidos es simplemente, micropéptidos, para distinguirlos de los péptidos que provienen de alguna fracción de una proteína, como se mencionó en el caso de la insulina. En todo caso, se puso en evidencia que algunos ARNs han sido clasificados equivocadamente como ARN no codificantes (Cohen 2014; Makarewich et al. 2018). Por su tamaño, los micropéptidos resultan difíciles de identificar por técnicas convencionales como el Western-blot. Esta metodología requiere primero de una adecuada separación por electroforesis en un gel, y la identificación posterior con un anticuerpo que reconozca al micropéptido. No obstante, la espectrometría de masas –una metodología de gran exactitud y sensibilidad – junto con el perfilado de ribosomas, han posibilitado la identificación y caracterización de múltiples micropéptidos. Mientras la espectrometría de masas permite detectar y medir con gran precisión moléculas muy pequeñas como los micropéptidos, el perfilado de ribosomas consiste en analizar qué fragmentos de ARN están siendo traducidos por los ribosomas, lo que ofrece una “fotografía” del proceso de síntesis de proteínas en la célula.
Más allá de la definición una vez identificados, lo que sin duda nos interesa a los científicos, es saber para qué la célula produce este tipo de micropéptidos.
Los micropéptidos en la función celular
La información disponible sobre los micropéptidos aún es escasa, pero tenemos algunas pistas que sugieren que son piezas importantes para comprender la complejidad del cuerpo humano. En primer lugar, los micropéptidos muestran una amplia distribución en diversos tejidos. Además, la gran mayoría de los micropéptidos identificados están conservados en múltiples especies, lo que evidencia su importancia biológica. Por ejemplo, se han advertido micropéptidos en una amplia diversidad de organismos, desde procariotas como Escherichia coli, Salmonella entérica y Bacillus subtilis, hasta eucariotas como la planta Arabidopsis thaliana y los seres humanos.
Hoy en día se cuenta con una base de datos llamada “FuncPEP” en donde se agregan nuevos micropéptidos con un papel fisiológico confirmado por las técnicas disponibles. Hasta 2024, esta base reportó 152 micropéptidos funcionales. Por lo tanto, el alcance biológico de diversos micropéptidos todavía no se conoce por completo. Aun así, ya se ha visto que intervienen en un rango amplio de funciones celulares como metabolismo, biología del músculo, la inmunidad, desarrollo, proliferación, entre otros (Zheng y Xiang 2022). Aquí se citan algunos ejemplos de micropéptidos involucrados en enfermedades metabólicas asociadas con la obesidad y en la contracción muscular.
Un ejemplo de micropéptido que proviene de un RNA largo no codificante es regulina-célula beta y -célula neural (BNLN). Estudios recientes demuestran que BNLN tiene un papel central en la función de las células beta, encargadas de sintetizar la insulina en el páncreas (Li et al., 2021). La cantidad en la que se produce BNLN se ve limitada en animales alimentados con una dieta alta en grasa. En contraste, al aumentar la cantidad de BNLN en animales mediante ingeniería genética, se observa una secreción de insulina incrementada en animales, con independencia de la dieta. Con base en esta evidencia, los investigadores sugieren que BNLN podría ser un pieza importante en la regulación de la diabetes.
Otro micropéptido, de solo 56 aminoácidos, implicado en el funcionamiento del músculo es la mitoregulina (Mtln) que también proviene de un ARN largo no codificante (Chugunova et al., 2019). Hasta el momento se ha descrito que Mtln regula la beta oxidación, función elemental para que las células de músculo esquelético o cardíaco obtengan energía. Cuando inactivan la secuencia de este gen en ratones para quitar su función, se observa una menor eficiencia para obtener energía en forma de ATP de los ácidos grasos. Adicionalmente, estudios recientes también han demostrado que Mtln regula la depuración de triglicéridos mediante la liberación de ácidos grasos y la beta-oxidación en el tejido adiposo.
SMIM30, un micropéptido de 59 aminoácidos, interviene en la homeostasis metabólica sistémica (Ma et al., 2025). Estudios en ratones señalan que SMIM30 desempeña un papel clave como regulador negativo de la respuesta inflamatoria de los macrófagos en el tejido adiposo blanco. Su ausencia, mediante ingeniería genética, provoca resistencia a la insulina como consecuencia de una respuesta inflamatoria exacerbada por estas células inmunes.
Por otro lado, se han descrito algunos micropéptidos implicados en la contracción muscular tanto en el músculo esquelético como en el cardíaco. Por ejemplo, la mioregulina –compuesta por 46 aminoácidos-– controla la concentración intracelular de calcio mediante la inhibición de la proteína ATPasa de Ca2+ del retículo sarcoplásmico en el músculo esquelético (Anderson et al., 2015). El silenciamiento de MLN en ratones –es decir, el cese de su producción– provoca un mayor desempeño muscular, debido a que se incrementa la recaptura de Ca2+ por la ATPasa de Ca2+ del retículo sarcoplásmico. Por otro lado, DWORF, un micropéptido de 34 aminoácidos localizado en la membrana del retículo sarcoplásmico, interviene en la contracción muscular tanto del músculo esquelético como del corazón (Makarewich et al., 2018). DWORF promueve la actividad de la ATPasa de Ca2+ del retículo sarcoplásmico al desplazar sus inhibidores como la mioregulina. Si se aumenta la cantidad de DWORF en las células del corazón, específicamente en los cardiomiocitos, mediante ingeniería genética se puede aumentar la contracción cardíaca, lo que resulta de gran interés en enfermedades del corazón.
Finalmente, se ha descrito que el micropéptido LINC01013ORF interviene en la fibrosis cardíaca (Quaife et al., 2023). En fibroblastos cardíacos, la fibrosis inducida por TGFβ1 se asocia con una mayor expresión de este micropéptido. De forma similar, su sobreexpresión reproduce los mismos efectos ocasionados por TGFβ1, mientras que su inhibición reduce la activación de los fibroblastos. En conjunto, estos hallazgos destacan la relevancia de LINC01013ORF en los procesos de activación celular que conllevan a la fibrosis cardíaca.
En resumen, distintos ARN largos no codificantes pueden dar origen a micropéptidos que cumplen funciones clave en el organismo, como regular el metabolismo de la glucosa y los lípidos, así como la actividad del músculo esquelético y cardiaco (Tabla 1). Su estudio resulta especialmente relevante en las enfermedades metabólicas asociadas a la obesidad y en las cardiovasculares, ya que permite comprender mejor su fisiopatología y, con ello, abrir nuevas posibilidades para enfrentarlas.
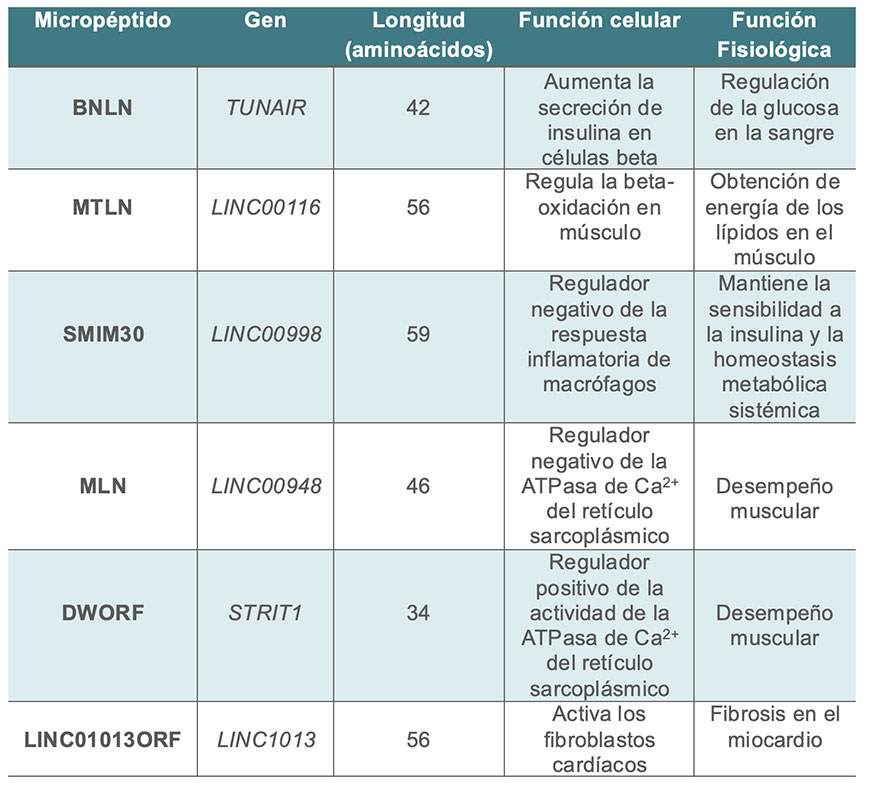
Tabla 1. Ejemplo de micropéptidos involucrados en el metabolismo y la función muscular.
Conclusión
Los secretos del genoma se han ido develando poco a poco, y el descubrimiento de los ARN largos no codificantes y sus micropéptidos asociados ha revolucionado nuestra percepción del llamado ADN "basura". La identificación y caracterización de estos micropéptidos no solo desafían nuestra comprensión tradicional de la biología molecular, sino que también prometen proporcionar un entendimiento más profundo de la complejidad de las células y organismos. Estos avances abrirán nuevas vías de investigación y aplicaciones potenciales en el estudio de diversas enfermedades.
Referencias
Anderson, D. M., Anderson, K. M., Chang, C. L., Makarewich, C. A., Nelson, B. R., McAnally, J. R., Kasaragod, P., Shelton, J. M., Liou, J., Bassel-Duby, R., & Olson, E. N. (2015). A micropeptide encoded by a putative long noncoding RNA regulates muscle performance. Cell 160(4), 595–606.
Chugunova, A., Loseva, E., Mazin, P., Mitina, A., Navalayeu, T., Bilan, D., Vishnyakova, P., Marey, M., Golovina, A., Serebryakova, M., Pletnev, P., Rubtsova, M., Mair, W., Vanyushkina, A., Khaitovich, P., Belousov, V., Vysokikh, M., Sergiev, P., & Dontsova, O. (2019). LINC00116 codes for a mitochondrial peptide linking respiration and lipid metabolism. Proceedings of the National Academy of Sciences of the United States of America 116(11), 4940–4945.
Cohen, S. M. (2014). Everything old is new again: (linc)RNAs make proteins! The EMBO Journal 33(9):937–938.
Li, M., Shao F., Qian, Q., Yu, W., Zhang, Z., Chen, B., Su, D., Guo, Y., Phan, A.V., Song, L.S., Stephens, S.B., Sebag, J., Imai, Y., Yang, L., Cao, H. (2021). A putative long noncoding RNA-encoded micropeptide maintains cellular homeostasis in pancreatic β cells. Molecular Therapy Nucleic Acids 26:307-320.
Makarewich, C. A., Baskin K.K., Munir A.Z., Bezprozvannaya S., Sharma G., Khemtong C., Shah A.M., McAnally J.R., Malloy C.R., Szweda L.I., Bassel-Duby R., y Olson E.N. (2018). MOXI Is a Mitochondrial Micropeptide That Enhances Fatty Acid β-Oxidation. Cell Reports 23(13):3701–3709.
Makarewich, C. A., Munir, A. Z., Schiattarella, G. G., Bezprozvannaya, S., Raguimova, O. N., Cho, E. E., Vidal, A. H., Robia, S. L., Bassel-Duby, R., & Olson, E. N. (2018). The DWORF micropeptide enhances contractility and prevents heart failure in a mouse model of dilated cardiomyopathy. eLife 7, e38319.
Zheng, X., y Xiang M. 2022. “Mitochondrion-Located Peptides and Their Pleiotropic Physiological Functions”. The FEBS Journal 289(22):6919–6935.
*Foto de portada creada con Chat GPT
Roxana Gutiérrez Vidal
Doctora en ciencias. Investigadora por México Secihti - Cinvestav Unidad Monterrey
roxana.gutierrezv@cinvestav.mx